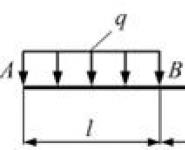
Нахождение железа в природе. Основные минералы и их свойства. Железо и его соединения Физические свойства железной руды
Цели урока:
Образовательная:
- На основании знаний учащихся о строении атомов металлов, об особенностях химической связи, свойствах металлов - простых веществ и их соединений, изучить особенности строения атома железа и проследить взаимосвязь строения атома железа, его свойств и свойств его соединений; познакомиться с важнейшими соединениями железа.
- Развить познавательный интерес к предмету, реализоватьмежпредметныесвязи курсов химии, биологии, истории, географии и литературы.
Развивающая:
- Развить умение учащихся анализировать, сравнивать, обобщать и делать выводы на основании уже имеющихся и вновь полученных знаний, как по химии, так и по другим дисциплинам.
- Прививать навыки поисковой и самостоятельной работы.
- Продолжить работу над формированием навыков по применению знаний при решении теоретических и практических задач (формирование предметной компетентности).
Воспитательная: Содействовать в ходе урока формированию научного мировоззрения, коммуникативной и информационной компетенции.
Тип урока: Урок усвоения новых знаний. Первичное закрепление новых знаний.
Форма организации учебной деятельности обучающихся: групповая, преобладающая работа - самостоятельная. Урок с элементамитехнологии критического мышления.
Оборудование: ПСХЭ, кристаллические решетки металлов, видеоролики, подтверждающие химические свойства железа и его соединений, реактивы (железо в порошке, сера, растворы соляной и серной кислот, сульфат меди, гидроксид натрия, красная и желтая кровяные соли, сульфат железа (II), хлорид железа (III),тиоционат калия),мультимедийное оборудование, диск с записью презентации, электронное пособие по теме "Металлы".
ХОД УРОКА
I. Организационный момент (1-2 мин)
1 стадия "Вызов".На этой фазе происходит актуализация знаний, имеющихся у учащихся, возникает интерес к обсуждаемому вопросу.
Краткое вступительное слово учителя (3 мин.).
Сегодня мы с вами продолжим путешествие в мир металлов: мы не только будем исследовать настоящее, но и заглянем далекое прошлое. Внимание посетителей Всемирной промышленной выставки в 1958 г в Брюсселе привлекло здание Атомиума.Девять громадных, диаметром 18 метров, металлических шаров, как бы парили в воздухе: восемь по вершинам куба, девятый в центре. Это была модель элементарной ячейки кристаллического альфа-железа, увеличенная в 165 млрд. раз (слайд 2)
Учитель объявляет тему урока:"Железо и его соединения" (слайд 3)
Прием "Покопаемся в памяти"
2 стадия - Осмысление новой информации. Учитель предлагает учащимся новую информацию, которую они должны усвоить. На этом этапе может быть предложена работа с текстом, заполнение матричной таблицы, чтение текста с пометками, выписка из текста.
Нахождение железа в природе.
Учащимся раздается печатный материал (Важнейшие природные соединения железа), демонстрируются минералы содержащие железо.
Работа с таблицей.
Ответить на вопросы: а) Какие классы неорганических соединений входят в состав железных минералов? б) Какой минерал имеет самое высокое значение массовой доли железа? в) В каких регионах России добывают железо?
Важнейшие природные соединения железа (слайд 4)
| Название минерала | Химическая формула | Содержание железа (в %) |
Важнейшие месторождения |
| Магнитный железняк (магнетит) |
Fe 3 O 4 | до 72 | Ю. Урал, Магнитогорск, КМА, Кольский п-ов |
| Красный железняк (гематит) |
Fe 2 O 3 | до 65 | Кривой рог, Сев. Урал, КМА |
| Бурый железняк (лимонит) |
2Fe 2 O 3 *3H 2 O | до 60 | Керчь, Ю. Урал, Карелия, Липецкая и Тульская обл. |
| Шпатовый железняк (сидерит) |
FeCO 3 | до 35 | Ю. Урал, КМА, Керчь |
| Серный колчедан (пирит) |
FeS 2 | до 47 | Урал, Алтай, Закавказье |
2. Физические свойства железа. Кристаллические решетки железа (слайд 5,6,7)
Прием "Кластер"
1. Напишите в середине листа ключевое выражение: "Физические свойства железа"
2. Начните записывать слова или предложения, которые приходят на ум в связи с данным заданием.
З. По мере того, как у вас возникают идеи, и вы записываете их, начните устанавливать те связи между идеями, которые вам кажутся подходящими.
4. Выпишите столько идей, сколько придёт вам на ум, пока не будут исчерпаны все ваши идеи.
На этом этапе урока возможно использование приема " Маркировочная таблица"(работая с текстом, учащиеся заполняют таблицу)например:
| "+" (знаю) |
"-" (Противоречит моему знанию) |
"V"
(Это для меня новое) |
"?" (Не понятно) |
| Простое вещество с металлической связью. Обладает пластичностью и ковкостью. | Железо символ планеты МАРС | Имеет 4 аллотропные модификации | |
| Железо проводит тепло и электрический ток. | Самый распространенный металл на Земле | ||
| Железо имеетметаллический блеск, обладает магнитными свойствами | Самый блестящий металл железо. | Свет поглощается поверхностью металла, и его электроны начинают испускать свои, вторичные, волны излучения. | Почему проводит тепло. |
3. Положение атома железа в периодической системе и строение атома (слайд 8)
26 Fe)))) d - элемент VIII-В группы, Аr = 56 1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2
4. Химические свойства железа (Слайд 9,10)
На этом этапе урока возможно использование приема "Самоанализ" с опорой на знания общих свойств металлов.
А) При нагревании взаимодействует со многими неметаллами:
* с кислородом 3Fe + 2O 2 = Fe 3 O 4
* c хлором 2Fe + 3Cl 2 = 2FeCl 3
* cсерой Fe + S = FeS
* c азотом 2Fe + N 2 = 2FeN
Б) Пары воды разлагаются раскаленным железом: 3Fe + 4H 2 O = Fe 3 O 4 + 4H 2
В)РазбавленныеHCL и H 2 SO 4 растворяют железо.
Fe + H 2 SO 4 = FeSO 4 + H 2 Fe + 2HCl = FeCl 2 + H 2
Г) С концентрированными азотной и серной кислотами при обычных условиях не реагирует (кислоты пассивируют металл)
Д) При нагревании реакция с концентрированной серной кислотой идет по уравнению 2Fe + 6H 2 SO 4 = Fe 2 (SO 4) 3 + 3SO 2 + 6H 2 O
Е) Взаимодействуетссолями: Fe + CuCl 2 = FeCl 2 + Cu
5. Свойства соединений Fe +2 и Fe +3 (слайд 11, 12)
| СОЕДИНЕНИЯ ЖЕЛЕЗА | ||
| +2 | +3 | |
| ОКСИДЫ | ||
| FeO - основный | Fe 2 O 3 - слабо амфотерный | |
| Общие свойства: 1. Не растворяются в воде |
||
| 2. Реагируют с кислотами | ||
| FeO+2HCl = FeCl 2 + H 2 O FeO + 2H + = Fe 2+ + H 2 O |
Fe 2 O 3 + 6HCl = 2FeCl 3 +3H 2 O Fe 2 O 3 + 6H + = 2Fe 3+ + 3H 2 O |
|
| 3. Реагируют с кислотными оксидами | ||
| FeO + SO 3 -> FeSO 4 | Fe 2 O 3 + 3SO 3 -> Fe 2 (SO 4) 3 | |
| 4. Реагируют с восстановителями | ||
| Fe0 + H 2 = Fe + H 2 O | Fe 2 O 3 + 3H 2 = 2Fe + 3H 2 O | |
| Различия: | ||
| 1. Неустойчивые соединения | 1.Реагируют с щелочами: Fe 2 O 3 +2NaOH -> 2NaFeO 2 +H 2 O Fe 2 O 3 +2KOH+3H 2 O=2K |
|
| Гидроксиды железа | ||
| Fe(OH) 2 - основный | Fe(OH) 3 - слабо амфотерный | |
| Общие свойства: | ||
| 1.Реагируют с кислотами: Fe(OH) 2 +2HCl=FeCl 2 +2H 2 O Fe(OH) 2 + 2H + = Fe 2+ + 2H 2 O 2.При t 0 разлагаются: Fe(OH) 2 = FeO + H 2 O |
1.Реагируютскислотами: Fe(OH) 3 +3HCl=FeCl 3 +3H 2 O Fe(OH) 3 + 3H + = Fe 3+ + 3H 2 O 2.При t 0 разлагаются: 2Fe(OH) 3 = Fe 2 O 3 + 3H 2 O |
|
| Различия: | ||
| 1.Окисляется на воздухе: 4Fe(OH) 2 +2H 2 O+O 2 =4Fe(OH) 3 |
1.Реагируют с щелочами: Fe(OH) 3 +KOH=K Fe(OH) 3 + OH - = - |
|
6. Лабораторные опыты. Качественные реакции на ионы Fe +2 , Fe +3 .
1. К раствору сульфата железа (II) - (FeSO 4) добавить несколько капель раствора гексацианоферрата (III) калия - красной кровяной соли K 3 . Наблюдаем выпадение осадка турнбулевой сини. Какого цвета?
Записать уравнение реакции:FeSO 4 +K 3 ->
2. К раствору хлорида железа (III) - (FeCl 3) добавить несколько капель раствора гексацианоферрата (II) калия K 4 - желтой кровяной соли. Отметить цвет осадка берлинской лазури. Записать уравнение реакции:
FeCl 3 + K 4 ->
3. К раствору хлорида железа (III) добавить несколько капель раствора тиоцианата калия (KCNS). Наблюдаем цвет раствора. Записать уравнение реакции:
FeCl 3 + KCNS ->
7. Практическое значение солей железа (слайд 13)
- FeSO 4 * 7H 2 O - железный купорос; применяется в текстильной промышленности при крашении тканей, в сельском хозяйстве для протравы семян и борьбы с вредителями сельского хозяйства, получение чернила.
- FeCl 2 - хлорид железа (II); применяется для получения чистого железа, компонент антианемических препаратов, катализатор в органическом синтезе.
- FeCl 3 - хлорид железа (III); применяется в технике как окислитель в производстве органических красителей, в текстильной промышленности - для протравки тканей при подготовке их к окраске, в медицине как кровоостанавливающее средство, компонент тонирующих растворов в фотографии, коагулянт при очистке воды, для определения фенолов.
- Fe 2 (SO 4) 3 - сульфат железа (III); применяется как химический реактив при гидрометаллургической переработке медных руд, как коагулянт при очистке сточных вод, для получения квасцов, пигмента Fe 2 O 3 .
3 стадия - Рефлексия, Размышление. Происходит осмысление всей информации, полученной на 2 стадии. Размышление и обобщение того, "что узнал"ребенок на уроке по данной проблеме. На этой стадии может быть составлен опорный конспект в тетради учащегося. Кроме того, могут быть осуществлены:
а) возврат к стадии вызова;
б) возврат к ключевым словам;
в) возврат к перевернутым логическим цепочкам;
г) возврат к кластерам.
Возможно использование приемов: "Перепутанные логические цепочки"
или "Синквейн":
- на первой строчке тема называется одним словом (существительным)
- вторая строчка - это описание темы в двух словах (прилагательных).
- третья строка-описание действия в рамках темы тремя глаголами.
- четвертая - это фраза из четырех слов, показывающая отношение к теме.
- пятая - синоним из одного слова, который повторят суть темы.
или "Конструирование текста" (слайд 14)
Задание: Из предложенных формул соединений составьте генетический ряд Fe +2 (для первого варианта) и генетический ряд Fe +2 (для второго варианта).
Fe(OH) 2 , Fe, Fe(OH) 2 , FeCl 3 , Fe 2 O 3 , FeCl 2 , FeO
8. Домашнее задание (слайд 14)
1. Написать уравнения химических реакций, с помощью которых можно осуществить следующие превращения:
Fe -> FeCl 3 -> Fe(OH) 3 -> Fe 2 O 3 -> Fe -> FeSO 4 -> Fe(OH) 2 -> FeOa Fe -> Fe 3 O 4
2. Написать уравнения реакций ступенчатого гидролиза раствора Fe 2 (SO 4) 3 .
3. В уравнении химической реакции расставить коэффициенты методом электронного баланса: Fe 2 O 3 + KOH + KNO 3 -> K 2 FeO 4 + KNO 2 + H 2 O
Цели
. Познакомить с положением железа
в периодической системе химических элементов
Д.И.Менделеева, строением атома, природными
месторождениями, соединениями, современными
методами получения, свойствами и применением
железа. Способствовать выработке у школьников
навыков коллективного труда и товарищеской
взаимопомощи.
Оборудование и реактивы
. Пробирки,
таблицы по доменному производству; растворы HCl и H 2 SO 4 ,
порошки Fe(OH) 2 и Fe(OH) 3 , железные опилки,
растворы желтой кровяной соли K 4
и красной кровяной соли K 3 .
Тип урока
. Элементы лекции, рассказ,
беседа.
ХОД УРОКА
Учитель
. Сегодня мы продолжим речь о
металлах, вы узнаете о положении железа в
периодической системе химических элементов, о
строении его атома, о химических свойствах
металла железа, его соединениях, получении и
применении, роли железа в развитии человеческого
общества. Какова роль железа в человеческом
обществе?
Ученик
. Железо сыграло большую роль в
развитии человеческого общества и не потеряло
своего значения в настоящее время. Из всех
металлов оно наиболее широко используется в
современной промышленности.
Первобытный человек начал использовать железные
орудия труда за несколько тысячелетий до нашей
эры. В те годы единственным источником этого
металла были упавшие на землю метеориты, которые
содержат довольно чистое железо. В середине 2-го
тысячелетия до
н. э. в Египте была освоена металлургия железа –
получение его из железных руд. Это событие стало
началом железного века в истории человечества,
который пришел на смену каменному и бронзовому
векам. На территории России начало железного
века относится к рубежу 2–1-го тысячелетий до н. э.
Учитель
. Каково распространение
железа в природе?
Ученик
. Железо – один из самых
распространенных элементов в природе. В земной
коре его массовая доля составляет 5,1%, по этому
показателю оно уступает только кислороду,
кремнию и алюминию. Много железа находится и в
небесных телах, что установлено по данным
спектрального анализа. В образцах лунного
грунта, которые доставила советская
автоматическая станция «Луна», обнаружено
железо в неокисленном состоянии
.
Учитель
. В виде каких соединений
железо встречается в природе?
Ученик
. Железо входит в состав
большинства горных пород. Для получения железа
используют железные руды с содержанием железа
30–70% и более.
(Пользуясь физической картой
России, ученик показывает и называет
месторождения соединений железа.)
Основными железными рудами являются:
– гематит
Fe 2 O 3
– содержит до 65% железа, такие месторождения
железа встречаются в Криворожском районе;
– лимонит
Fe 2 O 3 n
H 2 O
– содержит до 60% железа, месторождения лимонита
встречаются в Крыму, например керченское
месторождение;
– пирит
FeS 2 – содержит
примерно 47% железа, месторождения пирита
встречаются на Урале.
Учитель
. Как получают железо в
промышленности?
Ученик
. В настоящее время основным
промышленным способом переработки железных руд
является производство чугуна доменным
процессом. Чугун
– это сплав железа,
содержащий
2,2–4% углерода, а также кремний, марганец, фосфор,
серу. В дальнейшем большая часть чугуна
подвергается переделу в сталь. Сталь
отличается от чугуна главным образом меньшим
содержанием углерода (до 2%), фосфора и серы.
Учитель
. Большое внимание уделяется
разработке методов прямого получения железа из
руд без осуществления доменного процесса. В чем
преимущество прямого получения железа? Главное
состоит в том, что восстановление оксидов железа
можно проводить без участия металлургического
кокса. Его заменяют более дешевым и
распространенным топливом – бурым углем,
природным газом. При прямом получении железа
можно использовать и бедные железные руды, шлаки
других производств, содержащие железо.
Прямое восстановление железа проводят в слегка
наклоненных вращающихся печах, похожих на печи, в
которых получают цемент. В печь непрерывно
загружают руду и уголь, которые постепенно
перемещаются к выходу, противотоком идет
нагретый воздух, создается температура ниже
точки плавления железа.
Чтобы получить технически чистое железо прямым
восстановлением, руду подвергают обогащению. При
этом удается повысить массовую долю железа,
отделить пустую породу (куски железа легко
отделяются от шлака) и снизить содержание
вредных примесей (серы и фосфора). В процессе
обогащения руду измельчают в дробильных
установках и подают в магнитный сепаратор.
Последний представляет собой барабан с
электромагнитами, в который при помощи
транспортера подается измельченная руда. Пустая
порода свободно проходит через магнитное поле и
падает. Зерна руды, содержащие магнитные
минералы железа, намагничиваются и отделяются от
барабана позднее пустой породы. Такую магнитную сепарацию
можно проводить несколько раз.
Затем руду обогащают методом флотации
. Для
этого руду помещают в емкость с водой, где
растворяют флотационные поверхностно-активные
вещества, которые избирательно абсорбируются на
поверхности полезного минерала. В результате
абсорбции флотореагента частицы минерала не
смачиваются водой и в ней не тонут. Через раствор
пропускают воздух, пузырьки которого
прикрепляются к кусочкам минерала и поднимают их
на поверхность. Частицы пустой породы хорошо
смачиваются водой и оседают на дне емкости.
Обогащенную руду собирают с поверхности
раствора вместе с пеной. В результате содержание
железа в руде может быть повышено до 70–72%
.
Рассмотрим схему одного из способов прямого
получения железа. Процесс проводят в
вертикальной печи, в которую сверху подают
обогащенную руду, а снизу – газ, служащий
восстановителем. Этот газ получают сжиганием
природного в недостатке кислорода.
Восстановительный газ содержит 30%
СО, 55%
Н 2 ,
13%
Н 2 О и 2%
СО 2 . Следовательно,
восстановителями служат оксид углерода(II)
СО
и водород:
Fe 2 O 3 + 3СО = 2Fe + 3CO 2 ,
Fe 2 O 3 + 3H 2 = 2Fe + 3H 2 O.
Восстановление ведут при температуре
850–900 °С, что ниже температуры плавления
железа (1539 °С).
Для многих современных отраслей техники
требуется железо очень высокой степени чистоты.
Тогда очистку технического железа проводят карбонильным
методом. Карбонилы – это соединения металлов с
оксидом углерода(II) СО. Железо взаимодействует с
СО при повышенном давлении и температуре
100–200 °С, образуя пентакарбонил железа:

Пентакарбонил железа – жидкость, которую легко можно отделить от примесей перегонкой. При температуре около 250 °С карбонил легко разлагается, образуя порошок железа:
Fe(CO) 5 = Fe + 5CO.
Если полученный порошок подвергнуть спеканию
в вакууме, то получится металл, содержащий
99,98–99,999% железа. Зачем нужно получать металл
такой степени чистоты?
Ученик
. Железо высокой степени
чистоты нужно прежде всего для изучения его
свойств, т.е. для научных целей. Если бы не удалось
получить чистое железо, то не узнали бы, что это –
мягкий, легко обрабатывающийся металл. Химически
чистое железо намного более инертно, чем железо
техническое. Важной отраслью использования
чистого железа является производство
специальных ферросплавов, свойства которых
ухудшаются от присутствия примесей
.
Учитель
. Каковы же химические
свойства железа?
Ученик
. Химические свойства железа
обусловлены строением электронных оболочек его
атомов. Железо – элемент побочной подгруппы VIII
группы 4-го большого периода. Железо относится к
d-элементам, электронная формула атома имеет
окончание …3d 6 4s 2 . Железо в соединениях
проявляет степени окисления +2 и +3. Максимальная
степень окисления железа +6. Она проявляется в
ферратах – солях несуществующей железной
кислоты. Например,
Na 2 FeО 4 – феррат
натрия
.
Учитель
. Как реагирует железо с
кислородом?
Ученик
. В электрохимическом ряду
напряжений железо стоит левее водорода, т. е.
имеет более отрицательный стандартный
электродный потенциал. Поэтому железо легко
растворяется в соляной и разбавленной серной
кислотах с выделением водорода
:
Fe + 2HCl = FeCl 2 + H 2 ,
Fe + H 2 SO 4 (разб.) = FeSO 4 + H 2 .
Более концентрированную серную кислоту (40–60%)
железо восстанавливает до
оксида серы(IV):
Fe + 2H 2 SO 4 = FeSO 4 + SO 2 + 2H 2 O.
В серной кислоте еще более высокой
концентрации (от 80 до 100%) железопассивируется
– покрывается тонкой и прочной оксидной пленкой,
которая предохраняет металл от растворения.
Такое же явление пассивации наблюдается и в
сильно концентрированной азотной кислоте,
поэтому концентрированные серную и азотную
кислоты можно перевозить в железной таре.
С разбавленной азотной кислотой железо может
реагировать с образованием соли железа(II), а с
более концентрированным раствором кислоты –
соли железа(III) и различных продуктов
восстановления кислоты, например:
4Fe + 10HNO 3 = 4Fe(NO 3) 2 + NH 4 NO 3 + 3H 2 O,
3Fe + 8HNO 3 = 3Fe(NO 3) 2 +2NO + 4H 2 O,
Fe + 6HNO 3 = Fe(NO 3) 3 + 3NO 2 + 3H 2 O.
Учитель
. Вспомните, что называется
коррозией. Каковы ее последствия?
Ученик
. Коррозия – это разрушение
металла под действием окружающей среды.
Образование ржавчины можно представить в
следующем виде:
4Fe + 3О 2 + 6H 2 O = 4Fe(OН) 3 ,

Ржавчина отслаивается от поверхности
металла, имеет много пор, поэтому не предохраняет
металл от дальнейшей коррозии. Из-за коррозии
гибнет огромное количество железа и его сплавов.
В XIX в., когда не существовало надежных методов
борьбы с коррозией, от нее гибла половина
выплавляемого металла. В современных условиях от
коррозии гибнет 1/6 часть выплавляемого чугуна.
Поэтому борьба с коррозией – одна из важнейших
задач человечества
.
Учитель
. Обладают ли амфотерностью
соединения железа?
(На поставленный вопрос может ответить сам
учитель или заранее подготовленный,
интересующийся химией ученик.)
Гидроксид железа(III) амфотерен, т. е. проявляет
свойства основания в реакции с кислотами:
Fe(OH) 3 + 3HCl = FeCl 3 + 3H 2 O,
и кислотные свойства в реакциях с концентрированными растворами щелочей:
Амфотерный характер имеет и оксид железа(III), который реагирует и с кислотами, и с основными оксидами:
Fe 2 O 3 + 6HСl = 2FeCl 3 + 3H 2 O,
![]()
Учитель заостряет внимание учащихся на том, что
существуют характерные реакции на соединения
двухвалентного и трехвалентного железа,
сопровождая свой рассказ проведением опытов.
Учитель
. Для обнаружения ионов
железа(III) удобно применять комплексное
соединение железа, называемое желтой кровяной
солью или гексацианоферратом(II) калия
K 4 .
При взаимодействии ионов
(Fe(CN) 6) 4–
с ионами
Fe 3+ образуется темно-синий
осадок – берлинская лазурь:

Другое соединение железа – красная кровяная
соль или гексацианоферрат(III) калия K 3
является реактивом на ионы
Fe 2+ .
При взаимодействии ионов
(Fe(CN) 6) 3– с
ионами
Fe 2+ также образуется темно-синий
осадок – турнбулева синь:

Перечислите основные области применения
железа. Какое природное значение имеет железо?
(Учащиеся отвечают на поставленные вопросы,
учитель поясняет их ответы.)
Первый ученик
. Ферраты различных
металлов используют в современных отраслях
радиоэлектроники и автоматики
.
Второй ученик
. Необычные соединения
образует железо с водородом, азотом и углеродом.
Атомы этих неметаллов имеют размеры меньше
атомов железа и легко внедряются между узлов
кристаллической решетки металла, образуя
твердые растворы внедрения.

Твердые растворы внедрения внешне похожи на
металл, но их свойства сильно отличаются от
свойств железа. Большей частью это очень твердые
и хрупкие вещества. С водородом железо
образует гидриды
FeH и
FeH 2 , с азотом –
нитриды
Fe 4 N и
Fe 2 N, с углеродом –
карбид
Fe 3 С – цементит, содержащийся в
чугуне и стали
.
Третий ученик
. Железо – это металл,
использование которого в промышленности и быту
не имеет пределов. Широко распространена сталь в
современной технике. Оксиды и соли железа
применяют в производстве красок, магнитных
материалов, катализаторов, лекарственных
препаратов, удобрений
.
Четвертый ученик
. Без железа не может
функционировать организм человека, в нем
содержится около 3–4 г железа, из них в крови – 2 г.
Железо входит в состав гемоглобина.
Недостаточное содержание железа в организме
человека приводит к головной боли, быстрой
утомляемости и другим заболеваниям. Железо также
необходимо для роста растений. В целом по
значимости железо в настоящее время является
главным металлом
.
Для закрепления изученного материала учащимся предлагаются следующие вопросы .
1. Каково положение железа в периодической системе химических элементов?
2. Какие степени окисления проявляет железо в соединениях?
3. Какие соединения железа обладают амфотерными свойствами?
4. Как реагирует железо с азотной и серной кислотами различной концентрации?
5. Как отличить соединения двух- и трехвалентного железа?
6. Каково применение и значение соединений железа на современном этапе развития человечества?Если позволяет время, то можно закрепить рассмотренный материал по производству железа, используя следующие вопросы .
1. В чем преимущество прямого метода получения железа?
2. Для чего применяют обогащение руды?
3. Как обогащают руду методом флотации?
4. В чем основной смысл очистки технического железа карбонильным методом?
ЛИТЕРАТУРА
Книга для чтения по неорганической химии. Сост.
В.А.Крицман, М.: Просвещение, 1984;
Фельдман Ф.Г., Рудзитис Г.Е.
Химия. Учебник для
9 класса общеобразовательных учебных учреждений.
М.: Просвещение, 1999;
Хомченко Г.П.
Химия для поступающих в вузы. М.:
Высшая школа, 1993.
Которые принадлежат к группе железа, делят на теллурические (земные), возникающие в условиях земной коры,и космические, попадающие на земную поверхность в виде метеоритов.
Теллурическое - α-Fe . Синоним - феррит. Теллурическое встречается очень редко. Обычно содержит примеси Ni, Со, Сu, Pt и других элементов. - кубическая, вид симметрии - гексоктаэдрический. O h - m3m(3L 4 L⁶ 3 6L 2 9PC) Структурная ячейка содержит 2(Fe, Ni). Пространственная группа - 0⁹ h - Im3m. Структура теллурического железа представляет собой центрированный куб (тип металлического тантала) с а 0 = 2,8607.
Агрегаты и габитус. Кристаллы встречаются очень редко. Преобладают зерна неправильной формы.
Физические свойства
. Цвет теллурического железа стально-серый, блеск металлический, черта стально-серая, блестящая. Сильно выражены магнитные свойства и ковкость. Твердость - 4-5, плотность - 7-7,8. Диагностические признаки. Характерные признаки железа - магнитность и ковкость. Отличие от сходных минералов. От самородной платины отличается сильной магнитностью, плотностью, а также растворимостью в HNО 3 . Главные линии на рентгенограммах: 2,02; 1,430; 1,168. Искусственное получение. Железо получают при металлургических процессах из различных железных руд путем восстановления углеродом по реакции:
2Fe 2 О 3 + ЗС = 4Fe + ЗСО 2 .
Образование и месторождения . Теллурическое железо образует вкрапленность, а иногда сплошные массы в основных и ультраосновных породах. Оно также встречается в виде отдельных зерен в россыпях. По происхождению теллурическое железо может быть магматическим и поверхностным. В первом случае оно возникает при раскристаллизации основных и ультраосновных пород, во втором - под влиянием процессов выветривания. Считают, что железо изверженных пород выносится со значительных глубин земли либо восстанавливается в магме углеродом или органическими веществами, захваченными магмой во время интрузии. Образование железа при выветривании также происходит вследствие восстановления: при каменноугольных пожарах самородное железо, например, может возникать по той же реакции, что приведена для искусственного получения. Земное самородное железо в значительном количестве встречается только в базальтах острова Диско (Гренландия) в виде крупных глыб.
Оно известно также вблизи г. Касселя (Германия). Земное железо ассоциирует здесь с пирротином (Fe 1-n Fe 2
/ 3n S), троилитом (FeS) и когенитом (Fe 3 C). В России земное железо известно в некоторых пунктах Карелии и Урала и на Украине в базальтах Яновой Долины (Ровенская область). Практического значения все эти проявления не имеют.
Метеорное железо . Метеорное железо встречается значительно чаще, нежели теллурическое. Оно представлено двумя минералами, которые являются твердыми растворами никеля в железе - камаситом и тэнитом.
Состав и свойства метеорного железа
Минерал | Химический состав, % | Плотность |
|||
ао |
|||||
Тэнит ………….. | 93,1 75,3 | 24,4 | 2,859 3,590 | 7,3-7,87 7,8-8,2 |
|
Камасит
(от греч. камакс - балка, стержень) - главная часть железных метеоритов. Он образует правильные закономерные срастания больших балок, которые переплетаются между собой или прилегают одна к другой. Между балок зажат тэнит (от греч. тайния - лента, полоса).
В связи с разным отношением этих двух минералов к травлению HNО 3 (камасит травится легче, чем тэнит) на полированной поверхности метеоритов появляется структура в виде так называемых видманштеттовых фигур, что является диагностическим признаком метеорного железа. Находки метеорного железа многочисленны. Наиболее известно так называемое «Палласово железо», найденное в 1749 г. на горе Темир между Красноярском и Минусинском и описанное академиком Палласом (начальный вес «Палласового железа» составлял 688 кг).
Железными рудами называются горные породы, содержащие железо, извлечение железа из которых является экономически целесообразным. Минералов, содержащих железо, очень много, но в большинстве случаев или содержание железа в них невелико, или самый минерал встречается в природе в небольших количествах.
Имеющие наибольшее значение минералы, содержащие железо, могут быть разделены на следующие четыре группы в зависимости от их химического состава: 1) окислы железа; 2) углекислое железо; 3) кремнистое железо и 4) сернистые соединения железа. Названия и перечень этих минералов представлены в табл. 7.
Магнетит. Химическая формула магнетита (магнитного железняка) Fe3O4. В нем содержится 72,4% Fe и 27,6% O2. Цвет его темный, от серого до черного; минерал обладает магнитными свойствами. Сингония кубическая, вид симметрии гексооктаэдрический, твердость 5,5-6; уд. вес 4,9-5,2. Доля этого минерала в общей добыче железных руд невелика. Однако в некоторых металлургических районах, например на Урале или в Швеции, магнетитовые руды являются преобладающими.
В природных условиях магнетит, сохраняя свое кристаллическое строение, в той или иной степени окисляется. Содержание кислорода в магнитном железняке в этом случае уже не отвечает полностью формуле Fe3O4 или FeO*Fe2O3.
Обычно в рудах, образованных магнитным железняком, кроме магнетита, встречаются продукты его выветривания - полумартит и мартит. По классификации, принятой акад. М.А. Павловым. к магнитным железнякам относят такие руды, у которых отношение Feобщ/FeO менее 3,5 (вместо 2.333 в неокисленном магнитном железняке). К полумартитам относят руды с отношением Feобщ/FeO более 3,5 и менее 7 и, наконец, к мартитам - руды с отношением Feобщ/FeO более 7. И.А. Соколов, принимая те же цифры, берег вместо отношения Feобщ/FeO отношение Feобщ/FeFeO. Таким образом, приведенная классификация магнетитовых руд является условной.
Гематит. В химически чистой окиси железа содержится 70% Fe и 30°/о O2. В природе известны две полиморфные модификации окиси железа - устойчивая a-Fe2O3 (тригональной оингонии) и неустойчивая y-Fe2O3 (кубической сингонии), обладающая сильномагнитными свойствами и носящая название маггемита.
Гематит представлен первой модификацией. Цвет кристаллических разностей гематита железо-черный до стально-серого. Удельный вес гематита 5,0-5,3, твердость 5,5-6. Гематит составляет основу важнейших в мире месторождений железной руды. Связанные с породами различных геологических периодов, эти руды широко распространены в разнообразных видах. Многие из этих видов названы по их отличительным особенностям; например, красный железняк, оолитовый красный железняк, железистая слюда, красная стеклянная голова и т. д.
Бурые железняки. Долгое время считалось, что окись железа образует с водой следующие химические соединения: турьит - 2Fe2O3*H2O (66,31% Fe и 5,3% гидратной воды); гетит - Fe2O3*H2O (62,92% Fe и 10,1% гидратной воды); лимонит - 2Fe2О3*3Н2О (59,88% Fe и 14,43% гидратной воды); ксаитоондерит-Fe2O3*2Н2О (57,14% Fe и 18,36% гидратной моды); лимнит - Fe2O3*3Н2О (52,3% Fe и "25,3% гидратной воды).
В последнее время в результате рентгенометрических исследований установлено, что в действительности окись железа образует с водой одно химическое соединение с отношением Fe2О3:H2O = 1:1, обладающее определенной кристаллической решеткой. Все более богатые водой разности гидроокислов железа по существу являются гидрогелями, а не соединениями определенного состава. Они, как правило, содержат адсорбированную воду в различных количествах.
В современных учебниках по минералогии формулу гетита часто изображают в виде HFeO2 (учитывая, что Fe в гетите связано с гидроксилом), а формула лимонита (все гидроокиси железа, для которых Fe2O3:H2O > 1)-HFeO2*aq (aqua по-латыни вода). Турьит, по рентгенометрическим и термическим исследованиям, оказался смесью гетита и лимонита с гидрогематитом и, следовательно, не является самостоятельным минералам.
Сингония гетита - ромбическая, ромбодипирамидальный вид симметрии.
Цвет лимонита и гетита - темнобурый до черного. Твердость гетита 4,5-5,5, лимонита 4-1; удельный вес гетита 4,0-4,4, лимонита - колеблется от 3,3 до 4,0.
По физическому состоянию и внешнему виду различают много разновидностей бурых железняков: бурая стеклянная голова, обыкновенный бурый железняк, болотные и озерные руды и другие.
Карбонаты. Важнейшим представителем этой группы является минерал, называемый сидеритом, железным шпатом или шпатовым железняком; состав его определяется формулой FeCO3 (48,3% Fe и 37,9% CO2). Из изоморфных примесей чаще всего присутствуют углекислые марганец и магний. Сингония сидерита - тригональная. Цвет сидерита в свежем состоянии - желтовато-белый, сероватый, иногда с зеленым или буроватым оттенком. Твердость сидерита 3,5-4,5; удельный вес 3,9.
При выветривании сидерит окисляется с образованием лимонита, гетита.
Силикаты железа. Силикаты железа входят как примеси в состав некоторых железных руд. К силикатам железа относят много минералов, например группу хлоритов, одним из представителей которых является шамозит (примерная формула 4FeO*Al2O3*3SiO2*4H2O). Содержание FeO в этом силикате колеблется от 34,3 до 42,5%.
Из минералов других групп, содержащих силикаты железа, следует назвать нонтронит, состав которого определяется формулой: m {Mg3 [ОН]2} p {(Fe, Аl)2 2} nH2O, альмандин - Fe3Al23; а андрадит Ca3Fe23.
Сернистые соединения железа. Одним из минералов, представляющих эту группу, шляется пирит (серный колчедан, железный колчедан) FeS2, содержащий 46,7% Fe и 53,4% S. Вследствие высокого содержания серы минералы, содержащие сернистые соединения железа, в качестве железных руд не применяются. Пиритные или колчеданные руды добывают в значительных количествах для производства серной кислоты, при этом руды обжигают на воздухе. Во время обжига большая часть серы удаляется, твердый остаток в основном представляет собой окись железа и носит название пиритных огарков. Эти огарки после агломерации могут идти в доменную плавку.
Марказит представляет собой полиморфную разность FeS2 и имеет ромбическую сингонию (пирит имеет кубическую сингонию).
/ минерал Железо
Железо относится к группе самородных элементов. Самородное железо является минералом, имеющим земное и космогенное происхождение. Содержание никеля на 3 процента выше в земном железе, по сравнению с космогенным. Также содержатся примеси магния, кобальта и других микроэлементов. Самородное железо имеет светло-серый цвет с металлическим блеском, включения кристаллов редки. Это достаточно редкий минерал, обладающий твердость в 4-5 ед. и плотностью в 7000-7800 кг на метр кубический. Археологи доказали, что самородное железо использовалось древними людьми задолго до того, как появились навыки по выплавке металла железа из руды. Данный металл в своем первоначальном виде имеет серебристо-белый оттенок, поверхность стремительно покрывается ржавчиной при высокой влажности или в воде, богатой кислородом. Данная порода отличается хорошей пластичностью, плавится при температуре в 1530 градусов по Цельсию, из него без труда можно ковать изделия и производить прокатку. Металл обладает хорошей электро- и теплопроводностью, дополнительно его отличают от других пород магнитные свойства. При взаимодействии с кислородом поверхность металла покрывается образующейся пленкой, которая защищает его от коррозийного воздействия. А при содержании в воздухе влаги железо окисляется, и на его поверхности образуется ржавчина. В некоторых кислотах железо растворяется, и происходит выделение водорода. Железо оказало огромное влияние на развитие человеческого общества и продолжает цениться сегодня. Его используют на многих производствах. Железо помогло первобытному человеку освоить новые способы охоты, привело к развитию сельского хозяйства благодаря новым орудиям. Железо в чистом виде в те времена было частью упавших метеоритов. По сегодняшний день ходят легенды о неземном происхождении данного материала. Металлургия берет свое начало в середине второго тысячелетия до н.э. В то время в Египте освоили получение металла из железной руды. В чистом виде железо содержится в небесных телах. Металл был обнаружен в лунном грунте. Сейчас железо добывают из руды горных пород, и Россия занимает лидирующее место по добыче этого металла. Богатые залежи железной руды расположены в европейской части, в Западной Сибири и на Урале. Железо необходимо при производстве стали, которая имеет широкий диапазон применения. Практически в каждом производстве используется данный материал. Широко применяется железо в быту, его можно встретить в виде кованных изделий и чугуна. Железо позволяет придавать изделию различную форму, поэтому его используют при ковке и создании беседок, ограждений и других изделий. Пользуются железом все хозяйки на кухне, ведь изделия из чугуна, это не что иное как сплав железа и углерода. Посуда из чугуна равномерно нагревается, долго сохраняет температуру и служит не один десяток лет. В состав практически всех столовых приборов входит железо, а из нержавеющей стали изготовляют посуду и различные кухонные принадлежности и такие необходимые предметы, как лопаты, вилы, топоры и другие полезные приспособления. Широко используется данный металл и в ювелирном деле. Теллурическое железо содержит примеси никеля (Ni) 0,6—2%, кобальта (Со) до 0,3%, меди (Сu) до 0,4%, платины (Pt) до 0,1%, углерода; в метеоритном железе никель составляет от 2 до 12%, кобальт—около 0,5%, имеются также примеси фосфора, серы, углерода. Поведение в кислотах: растворяется в НNО3. Семейство самородного железа (по Годовикову) Группа самородного никеля Железо (англ. Iron, франц. Fer, нем. Eisen) - один из семи металлов древности. Весьма вероятно, что человек познакомился с железом метеоритного происхождения раньше, чем с другими металлами. Метеоритное железо обычно легко отличить от земного, так как в нем почти всегда содержится от 5 до 30% никеля, чаще всего - 7-8%. С древнейших времен железо получали из руд, залегающих почти повсеместно. Наиболее распространенны руды гематита (Fe 2 O 3 ,), бурого железняка (2Fe 2 O 3 , ЗН 2 О) и его разновидностей (болотная руда, сидерит, или шпатовое железо FeCO3
,), магнетита (Fe 3 0 4) и некоторые другие. Все эти руды при нагревании с углем легко восстанавливаются при сравнительно низкой температуре начиная с 500 o С. Получаемый металл имел вид вязкой губчатой массы, которую затем обрабатывали при 700-800 o С повторной проковкой. В древности и в средние века семь известных тогда металлов сопоставляли с семью планетами, что символизировало связь между металлами и небесными телами и небесное происхождение металлов. Такое сопоставление стало обычным более 2000 лет назад и постоянно встречается в литературе вплоть до XIX в. Во II в. н. э. железо сопоставлялось с Меркурием и называлось меркурием, но позднее его стали сопоставлять с Марсом и называть марс (Mars), что, в частности, подчеркивало внешнее сходство красноватой окраски Марса с красными железными рудами.История появления железа
Где добывают железо?
Области применения
Химический состав
В природе существует несколько модификаций железа - низкотемпературная имеет ОЦК ячейку (Im3m), высокотемпературная (при температурах > 1179K) ГЦК ячейку (Fm(-3)m). В больших количествах содержится в метеоритах. В железных метеоритах при травлении или нагреве проявляются видманштеттеновы фигуры.
Происхождение: теллурическое (земное) железо редко встречается в базальтовых лавах (Уифак, о. Диско, у западного берега Гренландии, вблизи г. Касселя Германия). В обоих пунктах с ним ассоциируют пирротин (Fe1-xS) и когенит (Fe3C), что объясняют как восстановление углеродом (в т.ч. и из вмещающих пород), так и распадом карбонильных комплексов типа Fe(CO)n. В микроскопических зернах оно не раз устанавливалось в измененных (серпентинизированных) ультраосновных породах также в парагенезисе с пирротином, иногда с магнетитом, за счет которых оно и возникает при восстановительных реакциях. Очень редко встречается в зоне окисления рудных месторождений, при образовании болотных руд. Зарегистрированы находки в осадочных породах, связываемые с восстановлением соединений железа водородом и углеводородами.
Почти чистое железо найдено в лунном грунте, что связывают как с падениями метеоритов, так и с магматическими процессами. Наконец, два класса метеоритов - железокаменные и железные содержат природные сплавы железа в качестве породообразующего компонента.
Группа самородного железа
< 2,9, редко до 6,4 ат. % Ni - феррит
< ~ 6,4 ат. % Ni - камасит
> 24 ат. % Ni - тэнит
62,5 - 92 ат. % Ni - аваруит Ni3Fe
(Ni, Fe) - Самородный никель
рассказать об ошибке в описании
Свойства Минерала
| Цвет | Стально-серый, серо-черный, на полированной поверхности белый |
| Цвет черты | Серо-черный |
| Происхождение названия | Обозначение химического элемента - от латинского ferrum, Iron – от староанглийского слова, означавшего этот металл |
| Место открытия | Qeqertarsuaq Island (Disko Island), Qaasuitsup, Greenland |
| Год открытия | известен с древних времён |
| IMA статус | действителен, описан впервые до 1959 (до IMA) |
| Химическая формула | Fe |
| Блеск | металлический |
| Прозрачность | непрозрачный |
| Спайность | несовершенная по {001} |
| Излом | крючковатый занозистый |
| Твердость | 4 5 |
| Термические свойства | П. тр. Точка плавления (чистого железа) 1528°С |
| Типичные примеси | Ni,C,Co,P,Cu,S |
| Strunz (8-ое издание) | 1/A.07-10 |
| Hey"s CIM Ref. | 1.57 |
| Dana (7-ое издание) | 1.1.17.1 |
| Молекулярный вес | 55.85 |
| Параметры ячейки | a = 2.8664Å |
| Число формульных единиц (Z) | 2 |
| Объем элементарной ячейки | V 23.55 ų |
| Двойникование | по {111} |
| Точечная группа | m3m (4/m 3 2/m) - Hexoctahedral |
| Пространственная группа | Im3m (I4/m 3 2/m) |
| Отдельность | по (112) |
| Плотность (расчетная) | 7.874 |
| Плотность (измеренная) | 7.3 - 7.87 |
| Тип | изотропный |
| Цвет в отраженном свете | белый |
| Форма выделения | Форма кристаллических выделений:плотные зерна с неправильными извилистыми очертаниями, плёнки, дендриты, изредка самородки. |
| Классы по систематике СССР | Металлы |